FLOT périopératoire par rapport à CROSS néoadjuvante en cas d’EC:télésurveillance en cas de NSCLC
Compte-rendu:
Dre Ine Schmale
L’étude ESOPEC a examiné la chimiothérapie périopératoire (FLOT) par rapport à la chimioradiothérapie néoadjuvante (CROSS) chez des patient·es atteint·es d’un adénocarcinome de l’œsophage (EC) résécable. Dans le cas d’un cancer colorectal métastatique avec instabilité des microsatellites ou défaut de réparation des mésappariements, l’étude CheckMate 8HW a comparé le traitement de première ligne par nivolumab plus ipilimumab à une chimiothérapie. Dans l’étude REACH PC, la consultation en ligne précoce de patient·es atteint·es d’un cancer bronchique non à petites cellules (NSCLC) a donné des résultats étonnants par rapport à une consultation en présentiel au cabinet médical.
Cancer de l’œsophage: la chimiothérapie périopératoire est préférable à la chimioradiothérapie néoadjuvante
Pour l’adénocarcinome de l’œsophage non métastatique, la résection de la tumeur reste le traitement de référence à visée curative. Un traitement multimodal permet de prolonger la survie globale des patient·es. L’étude ESOPEC a cherché à déterminer si les patient·es atteint·es de tumeurs de stade cT2–4a, cN+/– tiraient davantage profit d’une chimiothérapie périopératoire (schéma FLOT: 5-FU, leucovorine, oxaliplatine, docétaxel) ou d’une chimioradiothérapie néoadjuvante (schéma CROSS: 41,4 Gy, paclitaxel/carboplatine).1 Le critère d’évaluation primaire de l’étude était la survie globale (OS).
Entre février 2016 et avril 2020, un total de 438 patient·es de 25 centres en Allemagne ont été inclus·es dans l’étude ESOPEC. L’âge moyen était de 63 ans et 89% étaient des hommes. Les tumeurs étaient de stade T cT3–4 dans 80 à 82% des cas et de stade N clinique cN+ dans 78 à 82% des cas.
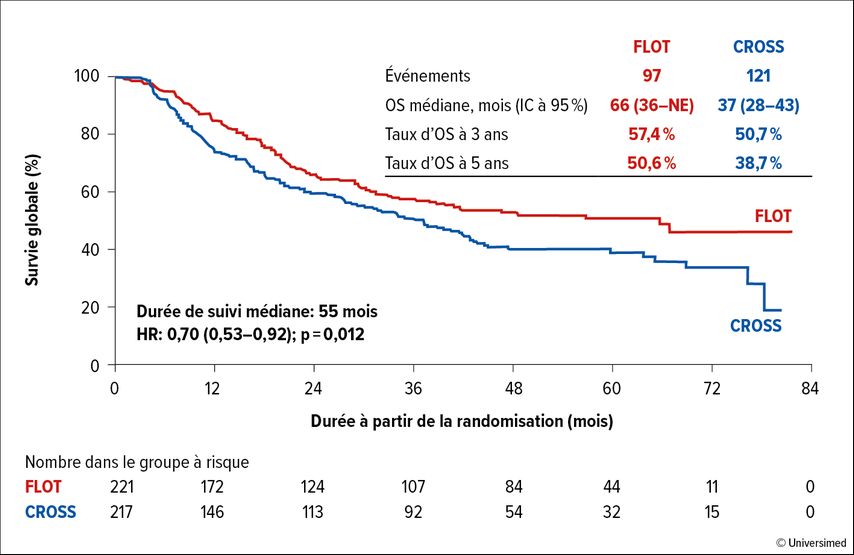
Au final, l’OS médiane, avec une durée de suivi de 55 mois, était de 66 (FLOT) par rapport à 37 mois (CROSS) (HR: 0,70; IC à 95%: 0,53–0,92; p=0,012; Fig. 1). Le taux d’OS était de 57,4% par rapport à 50,7% à trois ans et de 50,6% par rapport à 38,7% à cinq ans. Selon des analyses exploratoires de sous-groupes, les patient·es âgé·es <60 ans (HR: 0,57; IC à 95%: 0,34–0,95), les patient·es ayant une tumeur de stade T3–4 (HR: 0,68; IC à 95%: 0,50–0,92) et N+ (HR: 0,67; IC à 95%: 0,50–0,91) ont particulièrement bénéficié du schéma FLOT. La survie sans progression (PFS) médiane était de 38 mois par rapport à 16 mois, avec des taux de PFS à 3 et à 5 ans de 51,6% par rapport à 35,0% et de 44,4% par rapport à 30,9%, respectivement. Le risque de progression a été significativement réduit de 34% dans le bras d’étude FLOT par rapport au schéma CROSS (HR: 0,66; IC à 95%: 0,51–0,85; p=0,001). Une rémission pathologique complète (ypT0 ypN0) a été observée chez 16,8% par rapport à 10,0% des patient·es opéré·es. La mortalité postopératoire était de 1,0% par rapport à 1,7% (30 jours) et de 3,2% par rapport à 5,6% (90 jours).
Fig. 1: SG médiane sous chimiothérapie périopératoire (FLOT) par rapport à sous chimioradiothérapie néoadjuvante (CROSS) chez des patient·es atteint·es d’un adénocarcinome de l’œsophage non métastatique dans l’étude ESOPEC (modifié selon Hoeppner J et al.)1
Conclusion: La chimiothérapie périopératoire selon le schéma FLOT plus chirurgie prolonge l’OS par rapport à la chimioradiothérapie néoadjuvante selon le schéma CROSS chez les patient·es atteint·es d’adénocarcinome de l’œsophage de stade cT1cN+ et cT2–4a cN–/+ M0. La chimiothérapie périopératoire doit donc être privilégiée à la chimioradiothérapie néoadjuvante afin d’augmenter la probabilité de survie en cas de cancer de l’œsophage résécable.
CRC: de nouvelles données confirment le traitement de première ligne par nivolumab plusipilimumab
Les résultats de l’étude CheckMate 8HW ont montré que la PFS était significativement prolongée sous traitement de première ligne par nivolumab plus ipilimumab chez les patient·es atteint·es de cancer colorectal métastatique (mCRC) avec instabilité des microsatellites (MSI-H) ou défaut de réparation des mésappariements (dMMR). Lors du congrès annuel de l’ASCO, les résultats actualisés de l’efficacité de l’étude de phase III randomisée ouverte ont été présentés.2
Avec une médiane non atteinte et des taux de PFS à 12 et à 24 mois de 79% et 72%, respectivement, le risque de progression ou de décès a été significativement réduit de 79% dans le bras sous nivolumab plus ipilimumab par rapport à la chimiothérapie (PFS médiane: 5,9 mois; taux de PFS à 12/24 mois: 21%/14%; p<0,0001). Cet avantage a été confirmé pour tous les sous-groupes étudiés.
MESSAGE VIDÉO
Prof. Dre méd. Viola heinzelmann
Du nouveau sur le cancer de l’ovaire
AGO-OVAR 2.29/ENGOT: inhibiteur de points de contrôle + anti-VEGF en cas d’OC résistant au platine? – Combinaison d’inhibiteurs de points de contrôle en cas d’OC à cellules claires?
15% par rapport à 69% des patient·es dans les bras sous immunothérapie et sous chimiothérapie ont reçu un traitement ultérieur. 46% des patient·es du bras sous chimiothérapie sont passés dans le bras sous nivolumab plus ipilimumab après la progression de la maladie. La PFS sous traitement ultérieur (PFS2) médiane n’était pas encore atteinte pour les patient·es du bras sous immunothérapie et était de 29,9 mois pour les patient·es du bras sous chimiothérapie. Les taux de PFS2 à 12 et à 24 mois étaient respectivement de 89% par rapport à 65% et de 83% par rapport à 52%. La courbe de Kaplan-Meier a montré une réduction du risque de progression de 73% sous le traitement ultérieur (HR: 0,27; IC à 95%: 0,17–0,44). Le profil des effets secondaires diffère entre l’immunothérapie et la chimiothérapie. Malgré une durée de traitement plus longue sous nivolumab plus ipilimumab, les effets secondaires de grade 3/4 associés au traitement ont été moins nombreux dans le bras sous immunothérapie.
Conclusion: Les résultats actualisés de l’étude de phase III CheckMate 8HW confirment le traitement de première ligne par nivolumab plus ipilimumab pour les patient·es atteint·es de mCRC avec MSI-H/dMMR.
NSCLC: les patient·es bénéficient d’une télésurveillance précoce
Les patient·es atteint·es d’un cancer du poumon avancé font face à un lourd fardeau, que ce soit en raison des symptômes de la maladie, des effets secondaires du traitement, de la peur ou des soucis financiers. Une consultation palliative peut aider à gérer la maladie, mais l’accessibilité du cabinet médical et le temps nécessaire constituent des obstacles. C’est pourquoi la question a été posée de savoir si une consultation en ligne pouvait remplacer la consultation en présentiel.3
1250 patient·es atteint·es de cancer bronchique non à petites cellules (NSCLC) avancé ont eu une consultation mensuelle via un système en ligne ou se sont rendu·es dans un cabinet médical. L’âge moyen des patient·es était de 65,5 ans. Lors des consultations en ligne ou en présentiel, l’état général et les symptômes, la compréhension de la maladie et les décisions thérapeutiques ont été abordés à une fréquence similaire. La qualité de vie des patient·es (critère d’évaluation primaire de l’étude) s’est améliorée dans les deux bras au cours de l’étude et a même atteint de meilleurs résultats dans le groupe de télésurveillance. L’anxiété et la dépression ont diminué dans les deux bras, à nouveau plus fortement dans le groupe de télésurveillance. Ces résultats ont été obtenus malgré la présence plus fréquente des médecins de premier recours lors des consultations en présentiel qu’en ligne.
Conclusion: La prise en charge palliative précoce des patient·es atteint·es d’un cancer bronchique non à petites cellules a un effet positif sur la qualité de vie, que les consultations soient en ligne ou au cabinet médical.
Source:
ASCO Annual Meeting 2024, du 31 mai au 4 juin 2024, Chicago, IL, États-Unis, et en ligne
Littérature:
1 Hoeppner J et al.: Prospective randomized multicenter phase III trial comparing perioperative chemotherapy (FLOT protocol) to neoadjuvant chemoradiation (CROSS protocol) in patients with adenocarcinoma of the esophagus (ESOPEC trial). ASCO 2024; Abstr. #LBA1 2 Lenz HJ et al.: Nivolumab (NIVO) plus ipilimumab (IPI) vs chemotherapy (chemo) as first-line (1L) treatment for microsatellite instability-high/mismatch repair-deficient (MSI-H/dMMR) metastatic colorectal cancer (mCRC): expanded efficacy analysis from CheckMate 8HW. ASCO 2024; Abstr. #3503 3 Greer J et al.: Comparative effectiveness trial of early palliative care delivered via telehealth versus in person among patients with advanced lung cancer. ASCO 2024; Abstr. #LBA3
Das könnte Sie auch interessieren:
Sarcomes: des résultats prometteurs
Les sarcomes représentent une entité tumorale extraordinairement hétérogène et sont classés en plus de 100 sous-types selon l’OMS.1 Cela se reflète également dans les travaux de ...
AML au congrès de l’EHA: une grande déception et pourtant beaucoup d’espoir
La leucémie aiguë myéloïde a fait l’objet de nombreuses contributions lors du congrès 2024 de l’EHA. De nouvelles connaissances ont notamment été présentées sur la stratification du ...
Options sans chimiothérapie dans différents sous-groupes
Dans la prise en charge du cancer du sein avancé HR positif/HER2 négatif, on dispose désormais d’un paysage thérapeutique varié. Les approches ciblées, en plus de l’endocrinothérapie, ...